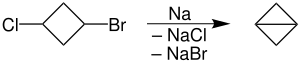雙環丁烷
化合物
雙環[1.1.0]丁烷(英語:Bicyclo[1.1.0]butane),簡稱雙環丁烷(英語:Bicyclobutane)是一種烴類化合物,化學式為C4H6。其是一種雙環分子,通過兩個環丙烷環通過順式融合得到,為無色易壓縮氣體[1]。雙環丁烷是可大規模分離的高環應力化合物中環應力最大的物質之一,其預估的環張力為63.9 kcal/mol。其為非平面分子,兩個三元環之間的二面角為123°[2]。
| 雙環丁烷 | |
|---|---|

| |
| IUPAC名 雙環[1.1.0]丁烷 Bicyclo[1.1.0]butane | |
| 識別 | |
| CAS號 | 157-33-5 |
| PubChem | 135973 |
| ChemSpider | 119751 |
| SMILES |
|
| InChI |
|
| InChIKey | LASLVGACQUUOEB-UHFFFAOYSA-N |
| 性質 | |
| 化學式 | C4H6 |
| 摩爾質量 | 54.09 g·mol−1 |
| 外觀 | 無色氣體 |
| 沸點 | 8.3 ± 0.2 °C |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
雙環丁烷首次被報導是出現在其乙酯衍生物C4H5CO2Et中。其通過對應溴代環丁烷羧酸酯在氫化鈉作用下發生脫鹵反應得到[2]。溴代環丁烷羧酸酯轉換成1-溴-3-氯環丁烷,然後在熔融金屬鈉作用下發生分子內武茲偶聯得到其雙環丁烷結構母體[1][3]。中間體1-溴-3-氯環丁烷也可以利用氯代環丁烷基甲酸採用溴和氧化汞進行改進的漢斯狄克反應得到[4]。
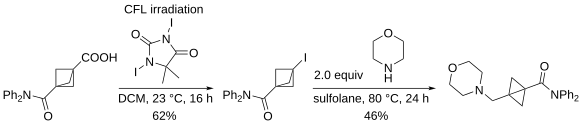
雙環丁烷衍生物的合成方法則是將適當取代的2-溴-(1-氯甲基)環丙烷在金屬鎂的四氫呋喃溶液中進行環合得到[5]。雙環丁烷的取代衍生物也可以利用碘代雙環[1.1.1]戊烷與胺、硫醇和亞磺酸鹽反應得到[6]。雙環[1.1.0]丁烷在藥物化學中常被用作共價反應基團[7]。
立體化學證據表明,雙環丁烷通過協同周環反應([σ2s+σ2a]環消除)熱解形成1,3-丁二烯,反應活化能為41 kcal/mol[8]。
生物合成
編輯α-亞麻酸可利用球孢魚腥藻(Anabaena sphaerica,菌株 PCC 7120)產生的融合蛋白轉化成雙環丁烷衍生物[9]。有的研究組報導一種定向演化的生物工程方法,使大腸桿菌表達出特定的工程血紅蛋白,使得雙環丁烷衍生物的產率和產速都得以優化[10]。
相關條目
編輯- 丙搭烯 (雙環丁二烯)
- [1.1.1]螺槳烷
- 雙環[1.1.1]戊烷
參考文獻
編輯- ^ 1.0 1.1 Wiberg, K. B.; Lampman, G. M.; Ciula, R. P.; Connor, D. S.; Schertler, P.; Lavanish, J. Bicyclo[1.1.0]butane. Tetrahedron. 1965, 21 (10): 2749–2769. doi:10.1016/S0040-4020(01)98361-9.
- ^ 2.0 2.1 Wiberg, K. B. Small Ring Bicyclo[n.m.0]alkanes. Hart, H.; Karabatsos, G. J. (編). Advances in Alicyclic Chemistry 2. Academic Press. 1968: 185–254. ISBN 9781483224213.
- ^ (1971) "Bicyclo[1.1.0]butane". Org. Synth. 51: 55.
- ^ (1971) "Mercury(II) oxide-modified Hunsdiecker reaction: 1-Bromo-3-chlorocyclobutane". Org. Synth. 51: 106.
- ^ D'yachenko, A. I.; Abramova, N. M.; Zotova, S. V.; Nesmeyanova, O. A.; Bragin, O. V. New synthesis of bicyclo[1.1.0]butane hydrocarbons. Bulletin of the Academy of Sciences of the USSR. 1985, 34 (9): 1885–1889. S2CID 96988412. doi:10.1007/BF00953929.
- ^ Mandler, Michael; Mignone, James; Jurica, Elizabeth; Palkowitz, Maximilian; Aulakh, Darpandeep; Cauley, Anthony; Farley, Christopher; Zhang, Shasha; Traeger, Sarah; Sarjeant, Amy; Paiva, Anthony; Perez, Heidi; Ellsworth, Bruce; Regueiro-Ren, Alicia. Synthesis of Bicyclo[1.1.0]butanes from Iodo-Bicyclo[1.1.1]pentanes. 2023-05-29. doi:10.26434/chemrxiv-2023-z8jvt-v2.
- ^ Tokunaga, Keisuke; Sato, Mami; Kuwata, Keiko; Miura, Chizuru; Fuchida, Hirokazu; Matsunaga, Naoya; Koyanagi, Satoru; Ohdo, Shigehiro; Shindo, Naoya; Ojida, Akio. Bicyclobutane Carboxylic Amide as a Cysteine-Directed Strained Electrophile for Selective Targeting of Proteins. Journal of the American Chemical Society. 2020-10-28, 142 (43): 18522–18531. ISSN 0002-7863. doi:10.1021/jacs.0c07490 (英語).
- ^ Woodward, Robert B.; Hoffmann, Roald. The Conservation of Orbital Symmetry. Angewandte Chemie International Edition. 1969, 8 (11): 781–853. doi:10.1002/anie.196907811.
- ^ Schneider, Claus; Niisuke, Katrin; Boeglin, William E.; Voehler, Markus; Stec, Donald F.; Porter, Ned A.; Brash, Alan R. Enzymatic synthesis of a bicyclobutane fatty acid by a hemoprotein lipoxygenase fusion protein from the cyanobacterium Anabaena PCC 7120. Proceedings of the National Academy of Sciences of the United States of America. 2007-11-27, 104 (48): 18941–18945. Bibcode:2007PNAS..10418941S. ISSN 1091-6490. PMC 2141887 . PMID 18025466. doi:10.1073/pnas.0707148104 .
- ^ Chen, Kai; Huang, Xiongyi; Kan, S. B. Jennifer; Zhang, Ruijie K.; Arnold, Frances H. Enzymatic construction of highly strained carbocycles. Science. 6 April 2018, 360 (6384): 71–75. Bibcode:2018Sci...360...71C. ISSN 1095-9203. PMC 6104391 . PMID 29622650. doi:10.1126/science.aar4239.